注意!口罩出口新規(guī)
出口企業(yè)應先取得我國醫(yī)療器械產(chǎn)品注冊證書,符合進口國(地區(qū))的質(zhì)量標準要求。如果您沒有取得醫(yī)療器械產(chǎn)品注冊證書,不建議進行口罩出口業(yè)務。
口罩企業(yè)及貿(mào)易商需注意,口罩出口需要提供這些資料信息 :
1:營業(yè)執(zhí)照(經(jīng)營范圍有相關經(jīng)營內(nèi)容)
2:企業(yè)生產(chǎn)許可證(生產(chǎn)企業(yè))
3:產(chǎn)品檢驗報告(生產(chǎn)企業(yè))
4:醫(yī)療器械注冊證(非醫(yī)用不需要)
醫(yī)療器械注冊,是指依照法定程序,對擬上市銷售、使用的醫(yī)療器械的安全性、有效性進行系統(tǒng)評價,以決定是否同意其銷售、使用的過程。它分為境內(nèi)醫(yī)療器械注冊和境外醫(yī)療器械注冊,境外的醫(yī)療器械不管是一類,二類,三類都要到北京國家食品藥品監(jiān)督局辦理:境內(nèi)的一,二類醫(yī)療器械在當?shù)氐氖』蚴惺称匪幤繁O(jiān)督局辦理,三類的到國家食品藥品監(jiān)督局辦理。醫(yī)療器械注冊證是指醫(yī)療器械產(chǎn)品的合法身份證。
5:產(chǎn)品說明書(跟著產(chǎn)品提供)、標簽(隨附產(chǎn)品提供)
6:產(chǎn)品批次/號(外包裝)
7:產(chǎn)品質(zhì)量安全書(跟著產(chǎn)品提供)
8:產(chǎn)品樣品圖片及外包裝圖片
9:貿(mào)易公司須取得海關收發(fā)貨人注冊備案
各國注冊、認證信息:
1.美國NIOSH認證
2.美國FDA注冊
3.歐盟CE注冊
4.日本PMDA注冊
5.韓國KFDA注冊
6.澳大利亞TGA注冊
4月1日起 開始海關將會嚴查。空海運等需要正式報關的防疫物品,都要送檢,送檢達到國家標準才能出口,否則要沒收銷毀并可能追究法律責任。
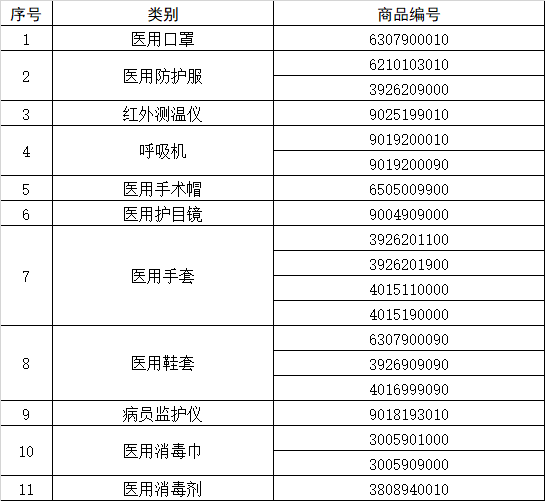
另外,海關總署10日發(fā)布2020年第53號公告,為加強醫(yī)療物資出口質(zhì)量監(jiān)管,按照《中華人民共和國進出口商品檢驗法》及其實施條例,海關總署決定對“6307900010”等海關商品編號項下的醫(yī)療物資實施。